
Ilustración por McCall Sarrett
Ya sea olvidando 20 años de su vida o teniendo la misma conversación cada cinco minutos para olvidarlo cada vez, el deterioro de la memoria puede tener un gran impacto en la vida cotidiana. Puede ser uno de los aspectos más confusos de la neurodegeneración y es un síntoma clave de la demencia.
Enfermedad de Alzheimer, también conocido como AD, es la forma más común de demencia, caracterizada por dificultades cognitivas y pérdida de memoria. Actualmente no existe una técnica clínica oficial para diagnosticar la EA, aparte de una autopsia. Sin embargo, hay dos características características del tejido cerebral de los pacientes con enfermedad de Alzheimer: beta amiloide (¿A?) placas y ovillos neurofibrilares, los cuales han proporcionado una gran cantidad de información sobre la patología de la neurodegeneración.
"Los nudos neurofibrilares surgen de un defecto en las proteínas llamadas proteínas tau".
¿A? es una proteína que resulta de proteolisis of Proteína Precursora De Amiloide (APP). Esto significa que APP se corta en fragmentos más pequeños, uno de los cuales es el A? fragmento. La APP es cortada en estos pedazos por enzimas llamadas secretasas, cuya función principal es escindir estas proteínas. Existen varias secretasas, pero hay una que es importante para la patología del Alzheimer: la gamma secretasa. La gamma secretasa produce una forma especial de A?: A?-42, la forma más tóxica de la proteína. Una vez descompuestos, estos fragmentos de proteínas comienzan a acumularse en el espacio exterior de las células. La clave de la toxicidad de estas proteínas es que se caracterizan por ser “pegajosas”, por lo que comienzan a formar agregados. Estos agregados continúan desarrollándose y pronto estas placas de beta amiloide están por todas partes, perjudicando en gran medida la función neuronal.
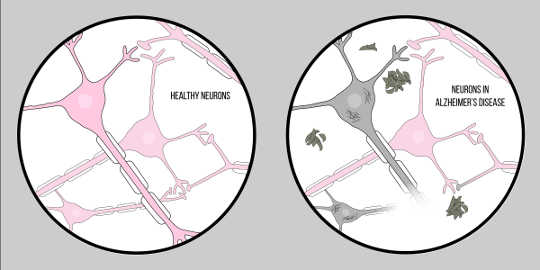 Figura de McCall Sarrett
Figura de McCall Sarrett
Este impacto de A? sobre la función neurológica ha llevado a la Hipótesis del amiloide, una teoría bien reconocida que propone una explicación para la neurodegeneración en el Alzheimer.
Ahora, para la segunda característica clave: los enredos neurofibrilares. Las marañas neurofibrilares surgen de un defecto en las proteínas llamadas proteínas tau. Las proteínas Tau sirven como un puente entre estructuras llamadas microtúbulos dentro de la célula. Los microtúbulos son moléculas de soporte que proporcionan forma y estructura a las células, específicamente, a los axones. Las proteínas Tau ayudan a estos microtúbulos a proporcionar estructura a los axones. Sin embargo, en el caso de La enfermedad de AlzheimerUna enfermedad neurodegenerativa caracterizada por la pérdida neuronal i ..., las proteínas tau se separan y acumulan en el cuerpo celular, también conocido como soma. Esto causa la degeneración de los axones, lo que dificulta aún más la comunicación de las neuronas. Esta dificultad en la comunicación neuronal es similar a los efectos de la beta amiloide; sin embargo, es importante tener en cuenta que estos enredos difieren mucho de las placas comentadas anteriormente en que influyen en la comunicación desde el interior de la célula en lugar de fuera.
"Los científicos aún no están seguros del mecanismo exacto responsable de la patología del Alzheimer".
Aunque ambos son extremadamente influyentes, ¿A? y tau no son los únicos factores relevantes en lo que respecta a la patología del Alzheimer. Los estudios han sugerido que la apolipoproteína E (APOE) gen puede ser tan influyente como A?. Hay tres variantes principales que codifican proteínas: ApoE2, ApoE3 y ApoE4. Se ha demostrado que ApoE4 se correlaciona con una disminución de la poda sináptica, mientras que ApoE2 produce un aumento. Ambas formas influyen astrocitos (importante células gliales dentro del sistema nervioso) y se correlacionan con su tasa de fagocitosis, el proceso por el cual el astrocitosLas células gliales en forma de estrella que tienen una serie de funciones, incluyendo ... engullen material celular. Cada variante de ApoE influye directamente en esta tasa de fagocitosis, ApoE2, que resulta en un aumento, y ApoE4, una disminución. Esto sugiere que los astrocitos pueden ser menos capaces de "limpiar" los escombros que flotan en la celda cuando se correlacionan con ApoE4. Por lo tanto, cuando estas placas se acumulan, el genotipo ApoE4 puede prevenir la eliminación de estos agregados, lo que contribuye a la degeneración.
Amiloide beta, tau y varios genes trabajan juntos para causar un problema de comunicación importante entre las células, que es esencialmente la enfermedad que conocemos como la enfermedad de Alzheimer. Dicha neurodegeneración es más común en áreas del cerebro asociadas con el aprendizaje y la memoria, pero con el tiempo se disemina por todo el cerebro. Con esta falta de comunicación viene una pérdida de sinapsis y, eventualmente, una disminución en la materia cerebral. Por lo tanto, es normal ver una disminución del tejido cerebral en una MRILa resonancia magnética, una técnica para ver la estructura ... a medida que avanza la enfermedad, revela que el Alzheimer literalmente encoge el cerebro. Nuestros modelos actuales de aprendizaje y memoria indican que las sinapsis desempeñan un papel clave en estos procesos, y brindan una posible explicación de cómo esta patología se correlaciona con los principales síntomas de la EA, como la pérdida de memoria.
Los científicos aún no están seguros del mecanismo exacto responsable de la patología del Alzheimer. Se han investigado muchos métodos innovadores en un intento por obtener un mayor conocimiento de este punto patológico, uno de los cuales son los biomarcadores de líquido cefalorraquídeo (LCR).
¿Niveles de A? y tau se puede medir en el LCR mediante un procedimiento llamado punción lumbar, que recolecta líquido cefalorraquídeo. ¿Mayores niveles de tau y niveles reducidos de A? se observan en pacientes con la enfermedad de Alzheimer. Este es el resultado de la A? acumulaciones en el cerebro, lo que a su vez resulta en una disminución de la concentración en el LCR. Estos datos sugieren que, en el futuro, los médicos y científicos podrán predecir el estado cognitivo de un paciente examinando los niveles de proteínas en el LCR.
Actualmente, no existe una cura definitiva para la enfermedad de Alzheimer. Sin embargo, el aumento del conocimiento de las proteínas patológicas involucradas, los genes asociados y la investigación científica en curso brindan la esperanza de un tratamiento efectivo en el futuro.
¿Qué avance crees que se necesita para que la medicina logre un tratamiento para el Alzheimer? Háganos saber en los comentarios!
Este artículo apareció originalmente en Conocer neuronas?
Sobre el Autor
Khayla Black es una estudiante de primer año en la Universidad de Nueva York en Shanghai y planea declarar una especialización en Ciencias Neurales con especialización en Ciencia de Datos con una concentración en inteligencia artificial. En el futuro, espera obtener un MD / PhD y convertirse en neurocientífica estudiando los aspectos moleculares del aprendizaje y la memoria. Durante su tiempo libre, a Khayla le gusta trabajar con la iniciativa MYELIN dentro de IYNA y leer cualquier material relacionado con la neurociencia. Además de estudiar neurociencia, le gusta correr, enseñar en escuelas primarias locales, resolver problemas de matemáticas y beber inmensas cantidades de café.
Libros relacionados
at InnerSelf Market y Amazon
Referencias
Lacor, PN, Buniel, MC, Furlow, PW, Clemente, AS, Velasco, PT, Wood, M., . . . Klein, WL (2007 de enero de 24). ¿A? Aberraciones inducidas por oligómeros en Synapse La composición, la forma y la densidad proporcionan una base molecular para la pérdida de conectividad en la enfermedad de Alzheimer. Recuperado de http://www.jneurosci.org/content/27/4/796
Murphy, MP y LeVine, H. (2010). La enfermedad de Alzheimer y el péptido ?-amiloide. ¿Revista sobre la enfermedad de Alzheimer?: JAD, 19(1), 311. http://doi.org/10.3233/JAD-2010-1221
O'Brien, RJ y Wong, PC (2011). Procesamiento de proteínas precursoras de amiloide y enfermedad de Alzheimer. Revisión anual de neurociencia, 34, 185-204. http://doi.org/10.1146/annurev-neuro-061010-113613
Chung, W.-S., Verghese, PB, Chakraborty, C., Joung, J., Hyman, BT, Ulrich, JD,… Barres, BA (2016). Nuevo rol dependiente de alelos para APOE en el control de la tasa de sinapsisConexiones entre las neuronas donde se transmite una señal desde ... poda por los astrocitos. Actas de la Academia Nacional de Ciencias de los Estados Unidos de América, 113(36), 10186-10191. http://doi.org/10.1073/pnas.1609896113
Zetterberg, H. (2009 de agosto de 19). ¿Amiloide? y APP como biomarcadores de la enfermedad de Alzheimer. Obtenido de https://www.sciencedirect.com/science/article/pii/S0531556509001594?via=ihub























