Los microbios intestinales en el intestino delgado son esenciales para una buena salud física y mental. Por Kateryna Kon / shutterstock.com
¿Podría la excrecencia de algunos pacientes con cáncer tener la clave para tratar ciertos cánceres en todas las personas?
¿Qué tiene que ver el cáncer con la caca? En los últimos años, investigadores de todo el mundo, incluidos nosotros, se han dado cuenta de que las bacterias intestinales (lo que llamamos el microbioma intestinal) de los pacientes con cáncer pueden ser la clave para mejorar las terapias contra el cáncer para los pacientes. Exactamente cómo sucede esto no está claro, pero puede estar relacionado con la capacidad de las bacterias intestinales para aumentar nuestra respuesta inmune natural.
El microbioma intestinal comprende toda la colección de microorganismos que viven en el tracto gastrointestinal. Pero la investigación reciente sugiere que los microbios en el intestino podrían no ser espectadores ociosos. Por el contrario, pueden ser fundamentales para ayudar a los pacientes a responder a nuevos medicamentos llamados "inhibidores del punto de control inmunitario" que ayudan a las células inmunes a reconocer las células tumorales y atacarlas. Mi objetivo como oncólogo que se especializa en melanoma es desarrollar nuevos enfoques para tratar el cáncer avanzado, particularmente en pacientes cuyos cánceres no responden a estas inmunoterapias de otro modo poderosas. Con este fin, decidimos investigar si ciertos tipos de microbios podrían aumentar la eficacia de los inhibidores del punto de control inmune y diseñar un único ensayo clínico para evaluar si el microbioma intestinal influye en la eficacia de estos medicamentos en pacientes con melanoma.
El microbioma intestinal y la inmunoterapia del cáncer
La comunidad médica sabe desde hace mucho tiempo que, si bien el sistema inmunitario puede "ver" las células cancerosas, a menudo no las destruye. Esto ocurre porque los cánceres pueden "esconderse" de las células inmunes, evitando así las respuestas anticancerígenas naturales generadas típicamente por el sistema inmune. Los cánceres sobreproducen proteínas como PD-L1 que muestran en su superficie para escapar de la vigilancia inmune. Las células cancerosas usan la proteína PD-L1 para esencialmente adormecer las células inmunes para dormir.
Los inhibidores de PD-1 y PD-L1 bloquean la interacción entre PD-L1 en la célula cancerosa y el receptor PD-1 en las células inmunes del cuerpo. Esto permite que el sistema inmunitario reconozca y mate estas células cancerígenas rebeldes.
Estos hallazgos fueron el resultado de décadas de arduo trabajo de científicos de todo el mundo, incluidos Tasuku Honjo en Japón y James Allison para cada año fiscal junto con la Arlene Sharpe y Gordon Freeman en los Estados Unidos. Su trabajo permitió a los científicos desarrollar fármacos como los llamados inhibidores de PD-1 y CTLA-4 que ayudan al sistema inmune natural del cuerpo a reconocer el cáncer como una entidad extraña, y al hacerlo, liberan una ola de células T que reconocen y matan las células cancerosas.
Estos agentes revolucionarios han transformado algunos cánceres avanzados en una enfermedad crónica; en el melanoma, los inhibidores de PD-1 producen respuestas duraderas en 30-40% de pacientes. Sin embargo, estos medicamentos no funcionan en el otro porcentaje 60-70 de pacientes con melanoma por un multitud de razones, incluyendo no tener los microbios correctos en el intestino, una condición llamada "disbiosis intestinal".
¿Cómo exactamente las bacterias en el intestino afectan el sistema inmune? Resulta que es complicado. El "microbioma intestinal" comprende aproximadamente 100 billones de células microbianas que superan en número a todas las células humanas en el cuerpo y forman un ecosistema que influye en la fisiología, la nutrición, el metabolismo y la función inmunitaria del huésped. Trabajo de varios grupos eminentes incluyendo Gustave Roussy, la Universidad de Chicago, la MD Anderson Cancer Center y Universidad de Texas en Dallas sugieren que no tener los errores correctos puede explicar por qué los inhibidores de PD-1 no funcionan al menos en algunos pacientes.
El microbioma intestinal y la inmunoterapia del cáncer
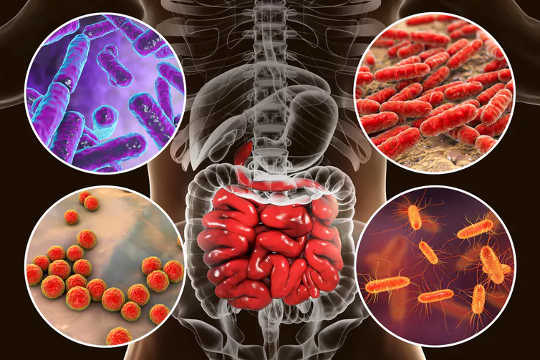 Esta ilustración muestra cuatro de las miles de especies que habitan en el intestino y constituyen el "microbioma intestinal". Por Kateryna Kon / shutterstock.com
Esta ilustración muestra cuatro de las miles de especies que habitan en el intestino y constituyen el "microbioma intestinal". Por Kateryna Kon / shutterstock.com
Analizar las bacterias intestinales es un trabajo duro. En todos los estudios publicados, los investigadores obtuvieron muestras de heces de pacientes con cáncer antes y después de la terapia inmune PD-1. Secuenciaron los genomas de las bacterias para descubrir sus identidades. Luego utilizaron diversas técnicas computacionales para calcular las especies exactas en cada una de las diversas muestras de heces, y para determinar la diversidad relativa y la abundancia de especies bacterianas entre los que respondieron (cuyos tumores se redujeron) y los pacientes que no respondieron. Varias estudios exploró el efecto de administrar materia fecal de pacientes respondedores humanos a ratones portadores de tumores y demostró que los tumores de ratón retrocedieron, lo que sugiere que algún elemento en la caca estuvo facilitando el tratamiento del cáncer.
Cuando vimos estos datos, nos preguntamos si la administración de microbios derivados de los respondedores -mediante un trasplante fecal- podría reducir los tumores al corregir el equilibrio de los microbios en el intestino, tal como lo hizo en los ratones portadores de tumores. Estábamos particularmente curiosos sobre si el abordaje podría usarse para tratar a pacientes que no responden a la inmunoterapia anti-PD-1. Aunque los diversos grupos, incluido el nuestro, estudiaron muestras de heces de pacientes con cáncer, las especies bacterianas asociadas con los pacientes respondedores variaron de un estudio a otro. Esto podría deberse a diferencias técnicas en los términos de cómo se recolectaron y analizaron estas muestras; pero también subraya las dificultades inherentes al análisis de si una sola especie bacteriana o un grupo de bacterias fueron responsables de la mediación de estos efectos.
Pero averiguar la bacteria exacta (o grupo de bacterias) responsable de este efecto puede llevar mucho tiempo. Hay 10-100 trillones de bacterias en el intestino humano, considerablemente más que el Techo de la deuda de los Estados Unidos a partir de 2018. Experimentar con una sola especie a la vez podría llevar décadas. En su lugar, decidimos utilizar "cócteles bacterianos" derivados de la materia fecal de pacientes con cáncer que lo habían hecho extraordinariamente bien en el tratamiento con PD-1.
Este enfoque toma ideas del mundo microbiano, en particular la importancia de la función sobre la identidad: lo que significa que lo que hace un microbio en particular, o una colección de microbios, es más importante que su identidad.
Primer ensayo en humanos
En nuestro primer ensayo en humanos, estamos recolectando el microbioma intestinal de pacientes cuyos cánceres han respondido extraordinariamente bien después de la inmunoterapia anti-PD-1. Al usar esto, generamos un trasplante de microbioma fecal: "FMT" o simplemente "un trasplante de popó".
Seleccionamos pacientes cuyos cánceres no respondieron a la inmunoterapia anti-PD-1. Después de una biopsia de su tumor, los pacientes reciben este "trasplante de caca" mediante una colonoscopía junto con un medicamento inhibidor de PD-1 llamado pembrolizumab. El trasplante fecal es seguido por varios tratamientos de pembrolizumab después de lo cual se evalúa la respuesta del paciente. Los pacientes que responden continúan recibiendo el medicamento para completar dos años de terapia.
Los vínculos entre las bacterias que hemos aislado y ciertos elementos de la dieta nos han llevado a controlar también los aportes dietéticos tanto en este estudio como en los pacientes que reciben inmunoterapia.
Los trasplantes fecales son altamente efectivos en el tratamiento de enfermedades potencialmente fatales Clostridium Difficile infecciones. La investigación que sugiere que la disbiosis intestinal puede ser la base de otras enfermedades ha engendrado una gran cantidad de estudios de trasplante fecal en otras enfermedades que van desde inflamatorio intestino enfermedad a obesidad y Enfermedad de injerto contra huéspede incluso en pacientes autistas con trastornos gastrointestinales.
Sin embargo, además de nuestro estudio, solo hay otro estudio en el Centro Médico Sheba en Israel que está probando este enfoque para tratar el cáncer avanzado.
![]() No sabemos si la manipulación del microbioma puede tratar el melanoma avanzado. Sin embargo, esperamos que nuestros esfuerzos de investigación avancen en la ciencia detrás del microbioma en pacientes con cáncer que reciben inmunoterapia y descubran nuevos vínculos entre el cáncer, la respuesta a la inmunoterapia del cáncer y el microbioma intestinal, incluidos los factores que podrían afectarlo, como la dieta y el ejercicio. Su popó puede ser crítico para este esfuerzo, así que considere donarnos una muestra.
No sabemos si la manipulación del microbioma puede tratar el melanoma avanzado. Sin embargo, esperamos que nuestros esfuerzos de investigación avancen en la ciencia detrás del microbioma en pacientes con cáncer que reciben inmunoterapia y descubran nuevos vínculos entre el cáncer, la respuesta a la inmunoterapia del cáncer y el microbioma intestinal, incluidos los factores que podrían afectarlo, como la dieta y el ejercicio. Su popó puede ser crítico para este esfuerzo, así que considere donarnos una muestra.
Sobre el Autor
Diwakar Davar, Profesor Asistente de Medicina, Universidad de Pittsburgh
Este artículo se publicó originalmente el La conversación. Leer el articulo original.
Libros relacionados:
at InnerSelf Market y Amazon























